達博生(shēng)物1類抗腫瘤新藥(E10A)聯用PD-1單抗方案Ⅱ期臨床試驗順利啓動!
2023-12-01
達博生(shēng)物1類抗腫瘤新藥(E10A)聯用PD-1單抗方案Ⅱ期臨床試驗順利啓動!
2023-12-01 10:34:27
11月28日,由廣州達博生(shēng)物制(zhì)品有(yǒu)限公司自主研發的治療用生(shēng)物制(zhì)品1類新藥“一項評價E10A聯合帕博利珠單抗對照帕博利珠單抗治療轉移性或不可(kě)切除的複發性頭頸鱗癌有(yǒu)效性和(hé)安全性的随機、開(kāi)放、多(duō)中心Ⅱ期臨床研究”項目啓動會(huì)在中山(shān)大(dà)學腫瘤防治中心內(nèi)科會(huì)議室圓滿開(kāi)展。
中山(shān)大(dà)學腫瘤防治中心內(nèi)科李志(zhì)銘教授團隊、特邀院內(nèi)頭頸科郭朱明(míng)教授、陳豔峰主任醫(yī)師(shī)、陳樹(shù)偉副主任醫(yī)師(shī)、放療科謝方雲教授、黃瑩主任醫(yī)師(shī)、陳春燕副主任醫(yī)師(shī)、超聲心電(diàn)科黎劍主任醫(yī)師(shī)、GCP機構李蘇主任等10餘位專家(jiā)教授、廣州達博生(shēng)物制(zhì)品有(yǒu)限公司董事長黃文林、CEO田爍、項目經理(lǐ)周傑彬及有(yǒu)關人(rén)員參與此次會(huì)議。

會(huì)上(shàng),項目PI李志(zhì)銘教授表示,頭頸部鱗癌目前治療可(kě)用藥物較少(shǎo),該項臨床研究前期已在治療頭頸部鱗癌方面進行(xíng)過多(duō)項臨床研究,本研究中由試驗藥物E10A聯合PD1使用,對于患者而言可(kě)能會(huì)有(yǒu)更好的療效。進行(xíng)該項藥物臨床試驗要嚴格遵守GCP相關規定,以高(gāo)度責任心和(hé)嚴謹的态度嚴格按照方案和(hé)流程進行(xíng)試驗;一定要保障受試者的合法權益,把受試者安全放在首位;做(zuò)好藥品管理(lǐ)和(hé)随訪,注意觀察療效,尤其是不良反應要及時(shí)按程序上(shàng)報,保證臨床試驗數(shù)據真實、準确、完整、及時(shí)、合法。
随後,臨床部經理(lǐ)周傑彬就該項目研究背景、研究簡介、試驗方案、觀察指标、藥物管理(lǐ)、樣本采集、入排标準、SAE、化驗檢查、風險控制(zhì)預案等進行(xíng)了詳細講解和(hé)培訓。專家(jiā)就知情同意、試驗藥品配制(zhì)、樣本采集及藥物使用操作(zuò)、藥品運輸保存等問題展開(kāi)了討(tǎo)論,達博生(shēng)物對研究者及專家(jiā)提出的疑問進行(xíng)專業解答(dá)并達成共識。達博生(shēng)物董事長黃文林教授對中山(shān)大(dà)學腫瘤防治中心的支持和(hé)幫助表示感謝,後續将全力支持和(hé)配合臨床試驗方面的各項工作(zuò)。E10A從基礎、理(lǐ)論、應用、臨床到最後的實施,都離不開(kāi)團隊合作(zuò)。我們需要團結一緻、齊心協力,夯實任務計(jì)劃,嚴格按照國家(jiā)标準執行(xíng)。

此次會(huì)議明(míng)确了臨床試驗的方案及分工,為(wèi)項目的開(kāi)展拉開(kāi)了帷幕。該項研究對于擴展頭頸部鱗癌治療的可(kě)用藥物範圍、提升現有(yǒu)抗腫瘤治療的療效有(yǒu)重要意義。達博生(shēng)物将以此為(wèi)契機,力争引入更多(duō)的藥物臨床研究項目,不斷推動新藥研究事業的發展,為(wèi)保障百姓用藥安全和(hé)有(yǒu)效貢獻力量。
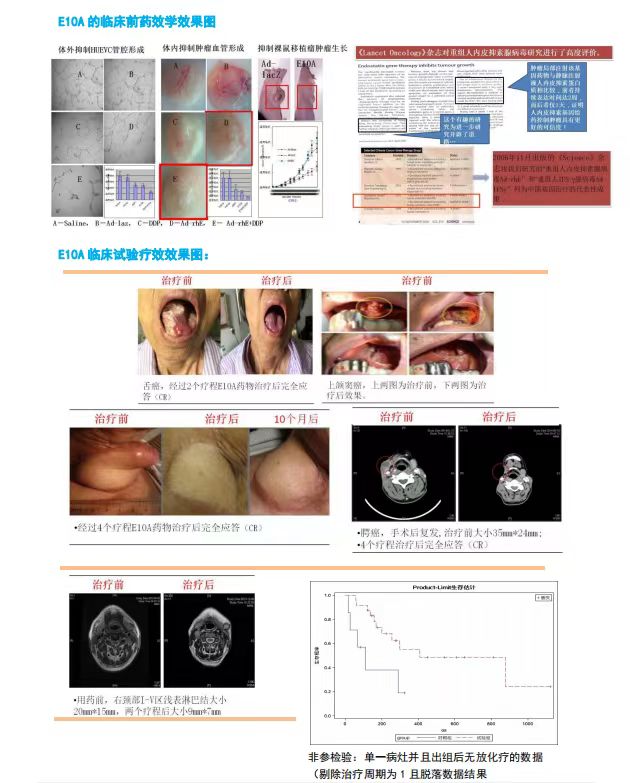
【關于E10A】

掃描二維碼分享到微信